
联系我们
江苏省超声诊断专业质量控制中心
联系人:殷林亮
电话:0512-62362333
地址:江苏省苏州市道前街26号 苏州市立医院超声诊断中心
江苏省介入超声操作规范及质量控制-2
2023-03-01介入超声是指在实时超声引导或监视下完成各种穿刺活检、抽吸、引流、置管、注药、硬化和消融等操作,是现代超声医学的重要分支,可分为介入性超声诊断和介入性超声治疗。
第一节 介入超声各类操作及诊疗规范
一、超声引导下穿刺活检操作规范
病理诊断是指导临床治疗的金标准,穿刺活检能够明确疾病的病理学诊断,评估疾病的预后和临床分期,辅助决定治疗方案。穿刺活检术由于有超声影像的监视和引导,取材过程动态实时,可清显示穿刺路径、刺针和病灶,操作简便,取材成功率高,安全,并发症少,无辐射,保护医患,是非手术条件下获取病理诊断的最常用方法。
(一)、诊疗流程规范
规范的穿刺活检流程对于确保穿刺活检的成功及安全至关重要。具体流程见下图。
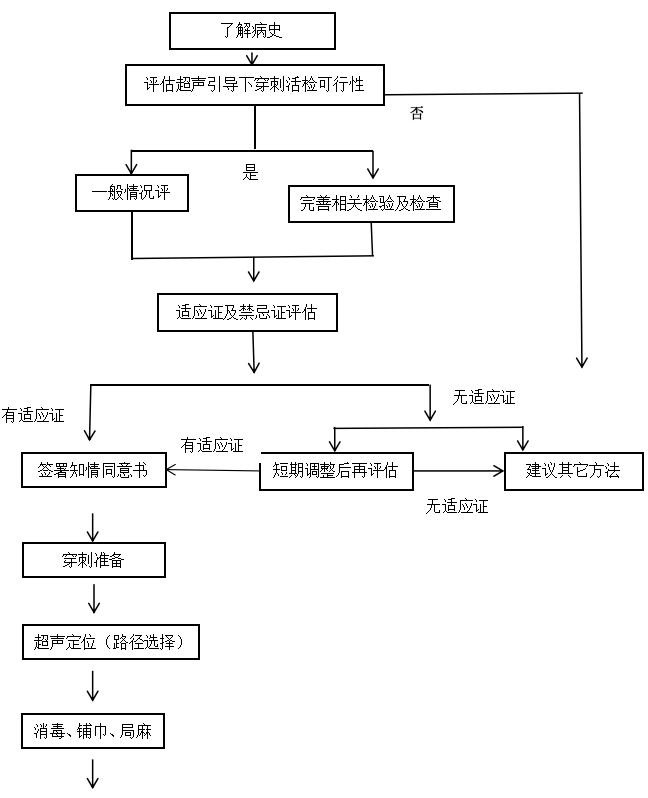
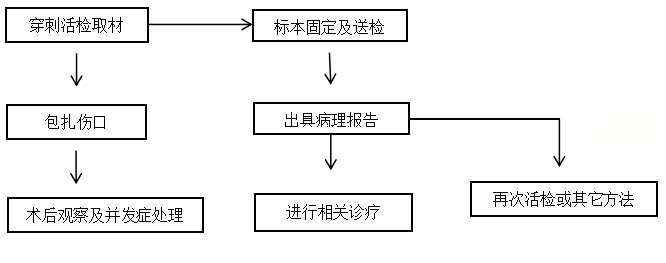
图 穿刺活检流程图
(一)、操作规范
1、选择体位
应以充分暴露所穿刺部位并能保持稳定为原则。
2、超声定位
选择安全路径,并测定穿刺针的进针深度和针芯弹出的距离,应以穿刺病灶距体表最近,开器、管管等重结构或器官为基本原则。
3、消毒、铺巾
体表穿刺部位皮肤消毒后铺无菌巾。
4、麻醉
皮内及沿进针路径做皮下局部麻配;局部麻醉下无法配合的患者,如/儿,必要时可行静脉麻醉。
5、穿刺活检取材
嘱患者配合,选取合适的呼吸状态,彩色多普勒血流成像再次确认所选定的刺路径,进针至靶目标预定位置,击发活检枪取材后出针,完成穿刺活检过程。
6、判断取材
依据标本形状、颜色及量决定取材次数。
7、处理标本
按各项病理检查要求进行标本固定,送检。通常使用 10%甲醛溶液固定,如拟做特殊检查需要专门的固定溶液。
8、术后处理
穿刺点处敷料包扎,必要时局部加压。
(二)、图像存储标准
1、动态图像存储
(1).穿刺活检靶病灶二维超声表现(纵切面和横切面)。
(2).穿刺活检靶病灶彩色多普勒表现。
(3).穿刺活检靶病灶与周围器官毗邻关系。
(4).超声引导穿刺活检靶病灶过程。
(5).超声引导穿刺活检术后观察靶病灶二维超声表现。
(6).超声引导穿刺活检术后观察靶病灶及针道彩色多普勒表现。
2、静态图像存储
(1).二维超声显示病灶最大切面及垂直切面。
(2).二维超声显示病灶最大切面及垂直切面的测量值。
(3).超声引导穿刺活检靶病灶过程静态图像。
(4). 超声引导穿刺活检术后观察靶病灶二维超声表现。
(5).超声引导穿刺活检术后观察靶病灶及针道彩色多普勒表现。
(四)、报告标准
超声引导穿刺活检检查报告一般包括患者基本信息、声像图、超声引导穿刺活检过程描述及超声穿刺活检检查提示。
以下为超声引导穿刺活检检查报告模板示例。
彩色多普勒超声引导病灶经皮穿刺活检术
操作过程:
患者平卧位/左侧卧位/右侧卧位,彩超引导下选择穿刺点,常规碘附消毒后铺孔巾,以1%盐酸利多卡因局部麻醉,手术刀切2mm 小口,避开彩色多普勒血流处,以18G/20G/16G穿刺针在彩超引导下,进针至病灶前缘取材,取出组织2/3/4条,送病理检查。
全部操作经过顺利,患者无不适反应。监测生命体征正常,观察30分钟,安返。
超声提示:彩超引导下病灶穿刺活检术。
二、超声引导针吸细胞学操作规范
针吸细胞学技术是通过细针穿刺病灶,吸取少许细胞成分做涂片检查的一种细胞病理学诊断方法。目前超声引导针吸细胞学技术具有操作简单、安全、取材准确、微确率高等优点,已广泛应用于直径小、高风险病灶的良恶性诊断,并成为重要的诊断方法。
(一)、诊疗流程规范同穿刺活检。
(二)、操作规范
1.选择体位
应以充分暴露所穿刺部位并能保持稳定为原则。
2.进针点选择
选择最短、安全的路径,以清晰显示穿刺靶目标,并避开邻近脏器、大血管等重要结构为基本原则;穿刺针宜在探头声束平面内进针,显示针道、针尖。
3.消毒、铺巾
严格遵守无菌原则,体表穿刺部位皮肤消毒(手术消毒范围应至术区15cm)后铺无菌巾。套探头保护套。
4. 必要时麻醉
穿刺点1%利多卡因皮下注射进行局部麻醉。甲状腺结节细针穿刺时一般不需麻醉,细针穿刺损伤小,多数患者可以耐受。
5.穿刺活检取材
选取合适的呼吸状态,彩色多普勒血流成像再次观察所选定的穿刺路径。操作者一只手固定超声探头,另一只手持穿刺针沿扫描平面斜行进针,实时观察进针过程。
6. 判断取材
当针尖到达病灶中心时停止进针,拔出针芯,开始快速、有效地提插,即在不同针道迅速提插5~10状负状态下),迅退针,保证操作时针尖对病变最大距离的切割,结束后用纱布压迫进针点。超声监测下对病变多角度、多位点穿刺,以保证样本的代表性。
7.处理标本
使注射器内充满空气,套上针头,将针头斜面向下对准载玻片,推动注射器活塞,将针具内的标本推射在载玻片的一端,并用另一块载玻片将标本均匀涂抹开,立即置于固定液中 10分钟。有条件者,建议病理科医生现场评估标本满意度,针吸细胞学技术的满意标本(以甲状腺结节为例)至少应有2张玻片且每张玻片有10保存完好的滤泡上皮细胞。有条件进行液基细胞学检测者,将穿刺针内残存的细胞置入液基液。
8. 穿刺针数
每个结节穿刺一般不超过4针。
9.术后处理
穿刺点处敷料包扎,有效压迫30分钟后确认有无出血(有效压迫:注意压迫的位置、面积、力度)。
(三)、图像存储标准同本章第三节。
(四)、报告标准
同超声引导穿刺活检技术。以下为甲状腺针吸细胞学活检技术报告模板示例。
彩超引导甲状腺结节穿刺细针活检术
操作过程:
患者平卧位/左侧卧位/右侧卧位,彩超下选择穿刺点,常规碘附消毒后铺孔巾,以1%盐酸利多卡因局部麻醉,避开重要血管,以CL 穿刺针在彩超探头引导下进针至病灶内行针吸,细胞涂片(3 张)、留置液基培养液,送病理检查、基因检测。
全部操作经过顺利,患者无不适反应。监测生命体征正常,观察30分钟,安返。
超声提示:
彩超引导下甲状腺结节穿刺针吸术。
建议:1.如病理及超声结果均为良性,请3~6个月后来我科超声随访。
2.如超声提示结节恶性可能性大,或甲状腺影像报告和数据系统TI- RADS4a、4b、5级,而细胞学病理为良性或为涂片见少量甲状腺上皮细胞及血细胞,建议再次穿刺。
三、超声引导置管引流操作规范
置管(引流)是临床常用的一种微创诊疗技术,通过体表解剖位置或影像引导将针具经皮肤穿刺至人体内的液性病变,完成抽液或置入引流管等操作,用于明确诊断(病原学、病理学等)、缓解症状或注入药物等诊断或治疗。彩超可实时清楚地显示体腔内液性病变、周围脏器及脏器内的血管和胆管等管道结构。因此,在实时超声的监视和引导下,可避开血管、胃肠道等重要结构,经皮穿刺至积液或管腔并置人引流管,尤其适用于积液量少、盲穿困难的患者。目前,超声引导置管引流已在临床上得到了广泛应用,具有操作简便、快速安全、成功率高等优点,且便于在床旁操作,因此已基本取代传统的通过体表解剖定位的盲穿置管方法。
(一)规范化流程
对于介入超声医师来说,不能仅把置管当作一项诊疗操作,而应在整个诊疗过程中关注患者的合并疾病及全身状态,充分权衡患者接受置管后可能的获益和风险,实现既完成置管操作、达到诊疗的目的,又提高患者的生活质量或延长生存期,同时最大限度减少并发症的发生,做到有效而安全。为此,超声引导置管应遵循规范化的诊疗流程,见下图 。
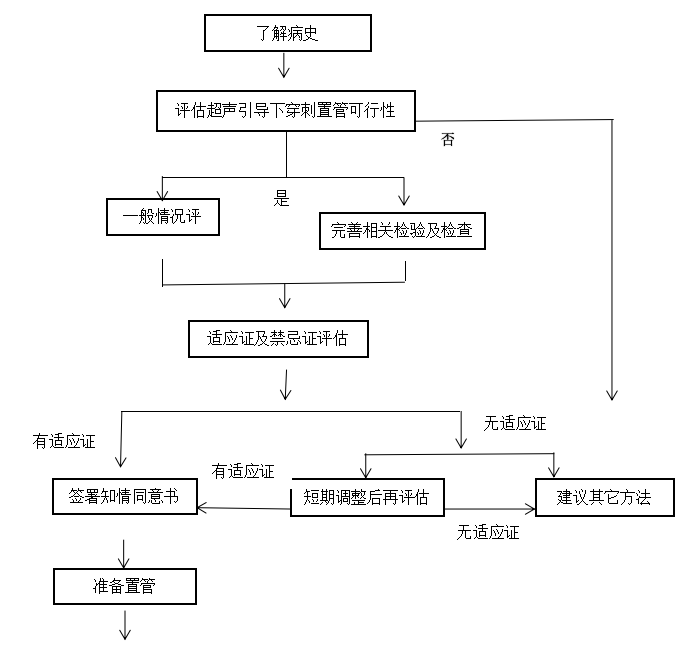
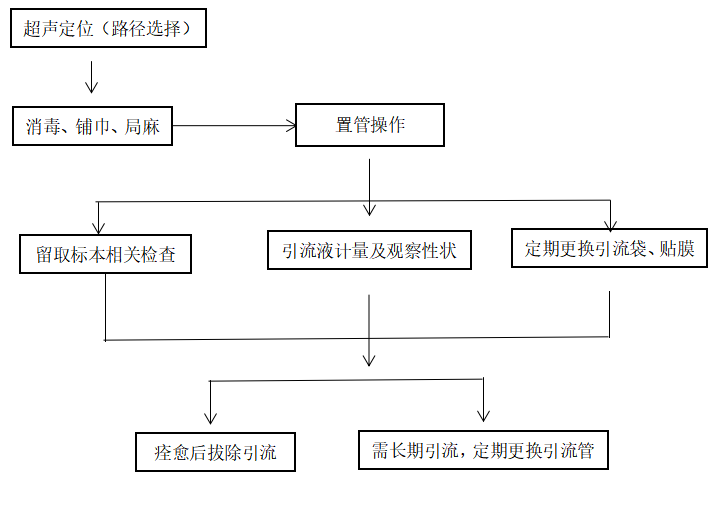
图 置管流程图
(二)操作规范化
1.患者体位
根据置管的部位确定适当的患者体位,如平卧位、左侧卧位、右侧卧位等必要时可采用靠垫辅助固定。
2.进针点选择
仔细进行超声检查,于皮肤完好部位选择合适进针点。进针点在平静呼吸状态下应可清楚地显示靶目标。如仅在吸气末或呼气末等特殊状态显示靶目标时应另外选择进针点。
3.无菌操作
严格无菌操作,消毒铺巾,进针点局部麻醉,根据需要进行皮肤切口。
4.进针前准备
进针前通过彩超再次确认路径安全,确保不经过较大血管或胆管等重要结构
5.操作方法及步骤
(1)两步置管法
实时超声引导穿刺(必要时请患者呼吸配合合),采用 Seldinger 技术进行置管操作,步骤如下:穿刺针针尖进入靶目标→退出针芯沿针鞘放入导丝→退出针鞘→扩张管扩张皮 肤、皮下组织至靶目标 >退出扩张管一沿导丝置入引流管→退出导丝→抽吸确认引流通畅→外固定引流管。该方法适用于较细管道,且置管成功率高,临床应用广泛。
(2)一步置管法
也称导管针经皮穿刺置管或一次穿刺插管术或Trocar 法,实时超声引导下穿刺,一次将带有金属针芯、金属内套管的引流管置人管道或病变部位,退出金属针芯、金属内套管,固定引流管即可。步骤如下:带有金属针芯、金属内套管的引流管进入靶目标→退出针芯及金属内套管抽吸确认引流通畅→外固定引流管。该方法操作简单,但较细管道或较小病灶不易置人,常用于较大病灶及较粗管道的置管。
6.术后处理
穿刺点处敷料包扎。
(三)图像存储标准
1.动态图像存储
1)穿刺置管靶目标二维超声表现(纵切面和横切面)。
2)穿刺置管靶目标彩色多普勒表现。
3)穿刺置管靶目标与周围器官关系。
4)超声引导穿刺置管靶目标过程。
5)超声引导穿刺置管置人扩张管过程。
6)超声引导穿刺置管置入引流管过程。
7)术后靶目标二维超声表现。
8)术后靶目标彩色多普勒表现。
2. 静态图像存储
1)二维超声检查靶目标最大切面及垂直切面。
2)二维超声检查靶目标最大切面及垂直切面测量值。
3)超声引导穿刺靶目标。
4)超声引导置入扩张管。
5)超声引导置入引流管。
6)术后穿刺路径及引流管二维超声表现。
7)术后靶穿刺点及引流管彩色多普勒表现。
(四)报告标准
超声引导置管报告一般包括患者基本信息、声像图、超声引导管引流过
程描述及超声引导置管引流检查提示。面及垂直切面。
2)二维超声检查靶目标最大切面及垂直切面测量值。
3)超声引导穿刺靶目标。
4)超声引导置入扩张管。
5)超声引导置入引流管。
6)术后穿刺路径及引流管二维超声表现。
7)术后靶穿刺点及引流管彩色多普勒表现。
(四)报告标准
超声引导置管报告一般包括患者基本信息、声像图、超声引导管引流过
程描述及超声引导置管引流检查提示。
彩色多普勒超声引导下置管引流术(一步置管法)
操作过程:
患者平卧位/左侧卧位/右侧卧位/坐位,彩超引导择点定位,常规消毒铺巾,1%盐酸利多卡因局部麻醉,避开彩色多普勒血流处,手术刀切 2mm小口,一步法将6F/8F引流管置入积液/脓腔/胆囊/扩张的胆管/扩张的肾孟内,退出针芯,引流管引流通畅,引流液为淡黄色/血性/脓性/……液体接引流袋固定。(术中共抽出引流液__ml,引流液送常规、生化、肿瘤标志物、细菌培养、查找肿瘤细胞……)
全部操作经过顺利,患者无不适反应。监测生命体征正常,观察30分钟,安返。
超声提示:
彩超引导下置管引流术。
彩色多普勒超声引导下置管引流术(两步置管法)操作过程:
患者平卧位/左侧卧位/右侧卧位/坐位,彩超引导择点定位,常规消毒铺巾,1%盐酸利多卡因局部麻醉,手术刀切2mm 小口,避开彩色多普勒血流处,以18G穿刺针置入积液/胆囊/扩张的胆管/扩张的肾盂/囊肿/脓肿内,置入导丝,退出引导针,扩张管扩张,置入6F/8F/10F/12F 引流管,退出导丝,引流管引流通畅,接引流袋固定。(术中共抽出引流液__ml,引流液送常规、生化、肿瘤标志物、细菌培养、查找肿瘤细胞……)
全部操作经过顺利,患者无不适反应,监测生命体征正常,观察30分钟,安返。
超声提示:
彩超引导下置管引流术。
四、超声引导囊肿抽吸硬化治疗操作规范
囊肿抽吸硬化治疗是通过超声引导将穿刺针经皮肤或经阴道穿刺至囊腔内,抽尽囊液后注入硬化剂,使囊壁细胞蛋白凝固变性,细胞坏死失去分泌功能,囊壁硬化闭合,达到临床治疗目的。在实时超声的监视和引导下穿刺囊肿并进行硬化治疗,操作简便、安全,无须住院,已经成为临床常用成熟技术,疗效确切,作为各脏器单纯性囊肿的首选治疗方法。
(一)规范化流程
囊肿硬化的规范化流程对于提高治疗效果,降低并发症的发生至关重要,流程见下图。
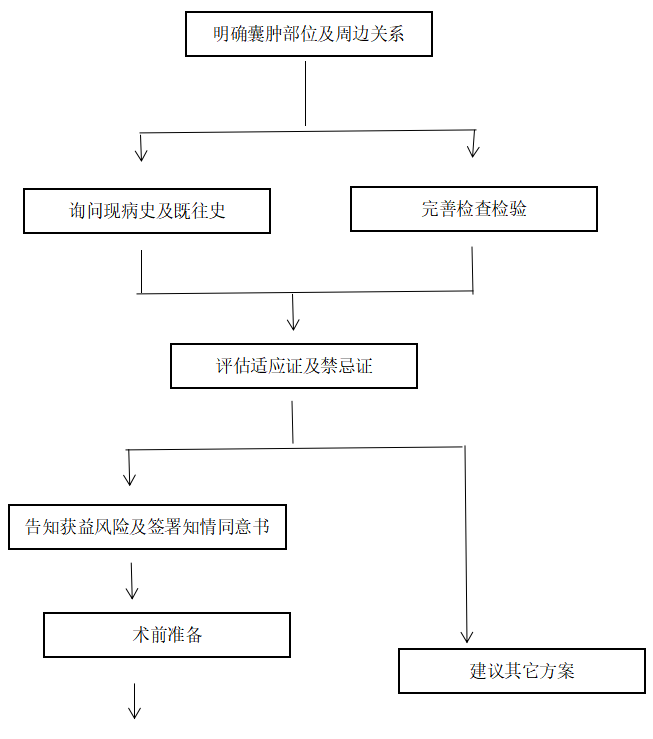
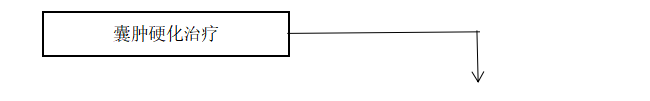
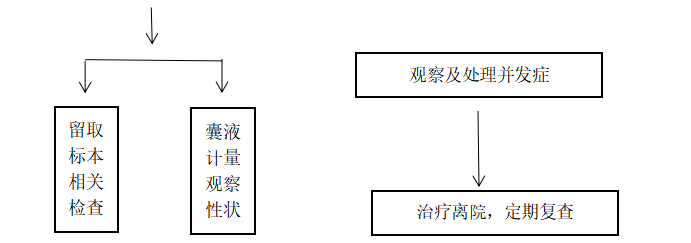
(二)操作流程
(1)固定患者体位:根据治疗部位选择易于操作且患者舒适的体位,以使患者能够更好地配合治疗。
(2)选择穿刺路径:超声仔细检查拟治疗的囊肿,确定穿刺点和进针路径,要求穿刺点皮肤完好,进针路径上能够避开血管、胆管、肠道等重要结构。超声检查脏器周边及腹盆腔有无游离液体,并记录。
(3)消毒铺巾:穿刺部位常规消毒铺巾。使用带有无菌保护膜和穿刺支架的探头再次确认穿刺点和进针路径。
(4)进针、抽液:穿刺点皮肤及皮下组织局部麻醉。实时超声引导将PTC针置入囊肿中心。拔除针芯,针鞘尾端接延长管并用注射器尽量抽尽囊液。记录抽出囊液的量和物理性状,如颜色、黏稠度、气味。依据囊液情况分别送常规、生化和病理细胞学检查。如怀疑合并感染时须送细菌培养和药敏。
(5)注人硬化剂:刚开始注射无水乙醇时应缓慢,观察患者有无剧烈疼痛或过敏等症状,同时超声实时观察囊腔充盈情况。注入硬化剂的量一般为抽出囊液体积的1/3~1/2,最大量不超过2/3 ,使药物充分与囊壁接触,破坏上皮细胞。若囊肿较大,一次注入硬化剂总量一般不超过150ml。硬化剂注人完毕后开始计时,建议依据囊壁厚度情况,无水乙醇保留3~5分钟,聚桂醇保留15~20分钟,之后全部抽出。对于硬化后抽出的硬化剂量与注入量基本一致时,一般进行两次硬化后结束治疗。若抽出量多于注入量的5%,需再次注入硬化剂进行硬化,直至抽出的硬化剂量与注人的量相等,治疗结束。
(6)治疗结束处理:针芯尾部接注射器,适当负压抽吸同时拔出穿刺针。局部消毒,无菌敷料覆盖,局部压迫5~10分钟。对于经阴道穿刺治疗的形态不规则的卵巢子宫内膜异位囊肿,治疗结束时可放回针芯后再拔针,以预防残留的无水乙醇沿针道外渗引起患者疼痛。治疗后观察30分钟后复查超声,重点关注治疗区局部及腹盆腔是否存在出血等异常表现。同时,观测患者生命体征无异常后,送回病房。
(三)图像存储标准
1.动态图像存储
1)穿刺囊肿二维超声表现(纵切面和横切面)。
2)穿刺囊肿彩色多普勒表现。
3)穿刺囊肿标与周围器官、血管和胆管等的关系。
4)超声引导穿刺囊肿的过程。
5)超声引导穿刺囊肿后抽液过程。
6)超声引导穿刺囊肿注入硬化剂过程。
7)术后靶目标二维超声表现。
8)术后靶目标彩色多普勒表现。
2. 静态图像存储
1)二维超声检查靶目标最大切面及垂直切面。
2)二维超声检查靶目标最大切面及垂直切面测量值。
3)超声引导穿刺靶目标。
4)超声引导抽液结束。
5)超声引导注入硬化剂。
6)术后穿刺路径及引流管二维超声表现。
7)术后靶穿刺点及引流管彩色多普勒表现。
(四)报告标准
超声引导囊肿硬化报告一般包括患者基本信息、声像图、超声引导管穿刺抽液过程、液体性状、注入硬化剂名称及量的描述及超声引导囊肿硬化提示。面及垂直切面。
彩色多普勒超声引导下囊肿硬化操作过程:
患者平卧位/左侧卧位/右侧卧位,彩超引导择点定位,常规消毒铺巾,1%盐酸利多卡因局部麻醉,避开彩色多普勒血流处,以19G/20G穿刺针置入目标囊肿内,,退出针心,连接延长管,抽出澄清/浑浊囊液200ml,注入聚桂醇注射液10ml。退针(囊液送常规、生化、肿瘤标志物、细菌培养、查找肿瘤细胞……)
全部操作经过顺利,患者无不适反应,监测生命体征正常,观察30分钟,安返。
超声提示:
彩超引导下囊肿穿刺硬化治疗术。
五、超声引导消融治疗操作规范
消融治疗是运用化学消融、能量消融(包括热消融与非热消融)等微创治疗技术,通过诱导肿瘤细胞的不可逆损伤而实现的肿瘤局部灭活方法。20余年来,影像引导的肿瘤消融已发展为一种被广泛认可的治疗手段,超声引导消融治疗包括经皮、术中和内镜超声引导等方式,以经皮途径为主。微波、射频、激光、高强度聚焦超声(HIFU)、不可逆电穿孔术(IRE)、冷冻及化学消融等多种技术已成功应用于肝脏、肾脏、肾上腺、乳腺、甲状(旁)腺、淋巴结、肺、骨子宫等多脏器肿瘤的治疗。消融治疗具有创伤小、疗效好、费用低、可重复、适用广等优势,尤其适合由于身体状况或心理因素无法耐受或不愿接受其他治疗的肿瘤患者,为广大患者提供了新的治疗选择。
(一)规范化流程
消融患者规范化流程见图
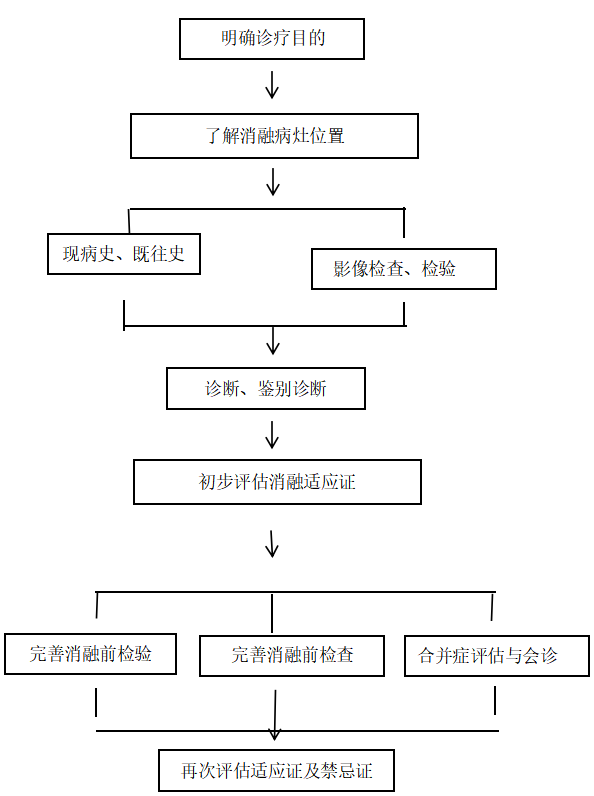
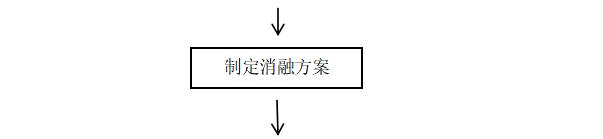
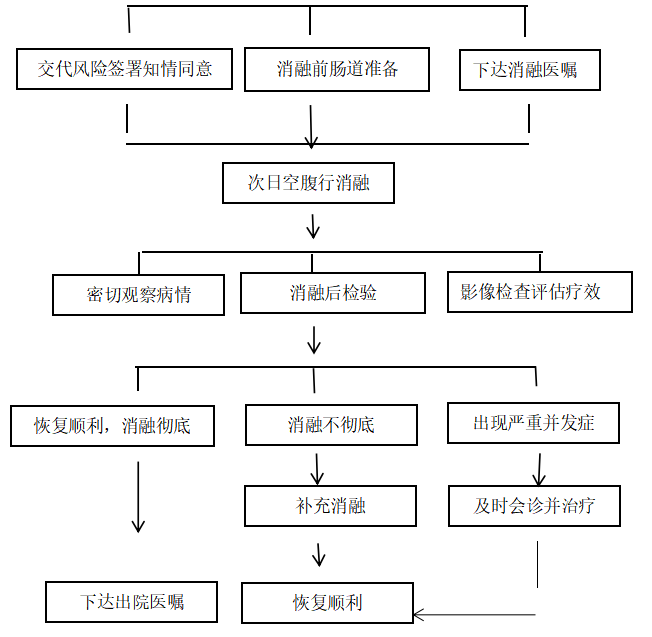
各脏器肿瘤消融前、中、后需要遵守规范及完整的诊疗流程,尽量使肿瘤灭活效果好,患者创伤小、恢复快并得到合理的综合治疗与随访指导,图 7-5-3主要围绕经皮消融进行阐述,适用于各种消融技术。
(二)操作规范
1.完善消融前检验
1)必查项目
血、尿、便常规及凝血功能、血型、血糖、血清传染病指标(乙型肝炎五项丙型肝炎抗体、艾滋病抗体、梅毒抗体)。
2)根据治疗脏器增加检验项目
内分泌指标(如醛固酮、皮质醇、甲状腺功能、甲状旁腺激素、性腺激素等)、血生化(肝肾功能、电解质)、肿瘤标志物、血气分析。
2.完善消融前检查
1)必查项目
心电图及胸片。
2)根据治疗脏器增加检查项目
相应脏器的CT/MRI检查,消融需要完善宫颈薄层液基细胞学检查(thin-cytologic test,TCT),前列腺消融需要完善尿动力试验,甲状旁腺消融需完善99mTc核素扫描。如患者经麻醉评估存在心肺疾病风险,需完善超声心动图、冠状动脉CT平板运动试验、肺CT肺功能等检查项目
3.评估消融治疗适应证及禁忌证
1)查看患者各项检查检验结果,评估异常结果是否可以纠正,是否影响消融治疗。
2)常规声或超声造影检查评估拟治疗病灶是否有合理安全进针路径及消融治疗必要性。
3)评估患者合并症是否影响消融治疗,必要时请相关科室会诊。
4)评估患者全身情况是否耐受消融治疗,可依据美国东部肿瘤协作组(Eastern Cooperative OncologyGroupECOG)分级或美国麻醉医师协会(Ameri can Society of AnesthesiologistsASA)分级。
4.制订消融方案
在完善各项检查及全面评估的基础上制订消融方案,包括是否进行肠道准备、药物(保肝、抑酸、降压、降糖、抗感染等)使用、其他相关学科会诊、明确消融预期目标(一次根治性、分次根治性或姑息性),采用的消融方式(微波、射频、激光、冷冻、HIFU、IRE)、布针方式、消融次数、消融肿瘤数目、辅助措施的应用(超声造影引导、人工腹水/胸腔积液/胆道注水、温度监测粒子植人、乙醇注射、三维消融规划、融合影像导航等)、采用的麻醉方式(静脉全身麻醉、局部浸润麻醉)、消融后血红蛋白尿的预估及水化、碱化尿液的预防处理等。
5. 签署知情同意书
消融前需与患者和家属充分沟通,了解患者及家属对病情的认知程度、对拟进行治疗结果的心理预期、对治疗存在风险的认知及接受程度。需向患者及家属充分交代患者病情、病灶情况、存在的其他治疗方式、治疗费用、治疗风险、能发生的意外及对风险、意外采取的防治措施等。在患者及家属充分了解上述情况后签署治疗知情同意书。
6.下达消融前医嘱
消融前1天须下达术前医嘱,包括拟行手术名称、术前禁食水、静脉通道的建立、肠道准备、消融进针部位皮肤准备。
7.实施消融
常规超声扫查确定肿瘤大小、形态、边界、部位、肿瘤血供和周边毗邻情况。行超声造影并结合增强MRI/CT 再次评估肿瘤大小形态和周边卫星灶情况,选择最佳穿刺路径,避开大血管、神经、胃肠、胆囊等重要结构进针,必要264造影操作规范
时训练患者屏气配合穿刺操作,依据病灶情况予以采用水隔离、测温、导航等辅助技术。消融时间、能量、电极数量参照各技术操作要点。
8.下达消融后医嘱
消融后下达术后医嘱,血常规是必查项目,静脉麻醉者还露检查尿、便常规和血生化指标以指导临床用药,依据消融脏器予以保肝保、肾药物,以及抗生素与饮食管理等医嘱,原则上一类切口消融脏器如甲状(旁)腺、乳腺、淋巴结、软切口疗无明确感染迹象者抗生素应用建议不超过3天。
9.观察消融后病情
消融治疗后常见的不良反应为疼痛,以治疗区附近为主,肝脏消融后可能出现中上腹疼痛,多考虑反射性或长时间空腹导致,术后第2天疼痛会明显减轻,如果出现长时间或剧烈疼痛,需警惕出血、胃肠穿孔、胆瘘等并发症发生;发热也是常见不良反应,但如果消融后长期高热不退,需警惕治疗区感染的口能,应及时根据实验室及影像检查明确诊断;如消融体积较大,个别敏感性体质术后当天可能会解浓茶色,甚至酱油色尿液,需及时予以水化、碱化尿液处理并密切观察肾功能改变;邻近膈肌病灶或肝硬化严重患者,消融后如果出现胸闷憋气症状,需及时超声检查明确胸腔积液、腹水情况,必要时可予引流。如果恢复顺利,无明显疼痛和发热等各种不适,静脉麻醉消融患者可3~5天后出院,局部麻醉治疗患者可次日出院,但如果出现各种严重并发症,需及时对症处理,必要时相关科室会诊。
10. 评价消融疗效
针对病变局部消融效果评价,主要应用影像学检查进行,以超声为基础评估手段,联合增强 CT/MRI 或超声造影检查,必要时用 PET/CT、PET/MRI检查,了解消融后凝固坏死范围及与肿瘤的覆盖关系,尤其是恶性肿瘤需明确原肿瘤是否完全坏死,有否残癌,决定是否需要补充消融治疗。良性病变的消融原则上以按照预定消融方案顺利完成消融并达到临床预期疗效作为成功标准。恶性肿瘤消融疗效评判标准参照国际消融规范化术语总结如下:
1)技术成功
肿瘤按照预定消融方案完成治疗。2)技术有效
消融后1个月增强影像评价肿瘤完全灭活。3)肿瘤残存
消融后1个月内经1~2 种增强影像评价,消融区边缘仍有肿瘤样增强,需进行补充治疗。
4)局部肿瘤进展
消融后1个月增强影像评价肿瘤完全坏死,患者进入随访期,在随访过程中如果消融区边缘出现肿瘤样增强,定义为局部肿瘤进展。
11.下达出院医嘱
患者出院前需对其出院后的检查、用药和复查予以详细、明确的指导。治疗前肿瘤标志物升高者需在消融后1个月复查;肝肾功能尚未恢复正常者需继续口服2周药物后复查生化指标;有感染风险者需配备口服抗生素。恶性肿瘤首次复查时间为术后1个月,如果有放化疗和内分泌治疗需要,嘱出院后于相关科室就诊;良性肿瘤首次复查时间为术后3个月。出院时告知患者诊治医师出诊时间,并留下联系方式,嘱如病情有变化及时与医生沟通。
12.定期随访
恶性肿瘤于消融后1个月进行首次复查,之后1年内每3个月复查1次,消融12个月以后视病情每3~6个月复查1次,以超声及相关检验为基础检查,根据复查结果,必要时结合超声造影、增强MRI/CT或PET/CT PET/MRI检查,目的是了解消融靶区的转归、有无残癌、局部肿瘤进展和远处转移,以及生存质量和生存时间。良性病变于消融后3、6、12个月行常规超声及相关实验室检查,根据复查结果,必要时结合超声造影或增强 MRI/CT检查,观察局部疗效。12个月后如治疗满意且病情稳定,可每年复查1次。
(三)图像存储标准
1.动态图像存储
1)消融靶目标二维超声表现(纵切面和横切面)。2)消融靶目标彩色多普勒表现。3)消融靶目标与周围器官关系。4)超声引导植入消融针过程。5)超声引导启动消融治疗过程。6)超声引导拔出消融针过程。
7)术后靶目标及消融针道二维超声表现。8)术后靶目标及消融针道彩色多普勒表现。
2. 静态图像存储
1)二维超声消融靶目标最大切面及垂直切面。2)观察消融靶目标与周围器官关系。3)超声引导植入消融针图像。4)超声引导启动消融治疗图像。5)超声引导拔出消融针图像。6)术后靶目标及消融针道二维超声表现。7)术后靶目标及消融针道彩色多普勒表现。
(四)报告标准
超声引导消融治疗报告一般包括患者基本信息、声像图、超声引导消融治疗描述、超声引导消融治疗提示及消融后注意事项。
以下为超声引导消融治疗检查报告模板示例。
病灶消融治疗记录
术前止血药物用药记录:
患者平卧位/左侧卧位/右侧卧位,彩超下选择穿刺点,常规碘附消毒后铺孔巾,以1%盐酸利多卡因进针点处皮下局部麻醉,避开彩色多普勒血流处,以微波/射频/激光消融针穿刺进入病灶内预定部位。
治疗编号: 疗程编号: 病灶编号:
机器类型:
病灶位置: 大小:
针数:根 治疗点数:
N1 位置: 能量:
N2 位置: 能量:
N3 位置: 能量:
N4位置: 能量:
N5 位置: 能量:
术中给药记录:
超声动态观察病灶区被强回声覆盖。
全部操作经过顺利。监测生命体征正常,观察30分钟,安返。超声动态观察病灶区被强回声覆盖。消融治疗后医嘱:
1. 卧床休息 小时。
2.绝对禁食水__小时,适当补液。
3.密切观察生命体征,注意出血倾向,浅表部位间断冷敷 24 小时。
4. 体温大于 38.5℃时,给予物理降温治疗。
5.4 小时后换纱布,平铺。
六、各项操作质量控制方案
1.操作规范质量控制
按照各治疗操作规范完成对靶目标及穿刺路径的检查,包括术前准备/操作步骤及标准切面图像存储。
2.存图标准质量控制
采取抽查报告内及工作站内图像存储两种方式进行存图标准质量控制。
报告存图合格率= 抽查报告存图合格例数x100%
总抽查报告例数
3报告书写规范质量控制
报告书写合格标准:符合报告书写要求,基本信息完整,描述与诊断规范,
内容完整,数据与文字无误。
报告书写合格率= 抽查报告书写合格例数x100%
总抽查报告例数
4.治疗成功率
超声引导消融治疗病例中,用消融治疗成功病例数占总消融治疗病例数的比例,判断超声引导消融治疗成功率。
治疗成功率= 治疗成功病例数 x100%
治疗病人总数
5.并发症发生率
超声引导穿刺治疗病例中,用发生并发症的病例数占总治疗病例数的比例,判断超声引导介入治疗的并发症发生率,可对轻微并发症和严重并发症分别统计。
超声引导穿刺治疗并发症发生率= 超声引导治疗发生并发症病例数x100%
总超声引导微创治疗病例数
6.超声引导囊肿穿刺成功率(12个月后体检缩小超过50%)
对所抽查的超声引导囊肿硬化病例中,用囊肿硬化成功病例数占总硬化病例数的比例,判断超声引导囊肿硬化的成功率。
超声引导囊肿硬化成功率=超声引导穿刺硬化成功病例数 x100%
总超声引导穿刺硬化病例数
7、超声引导穿刺活检取材合格率
超声引导穿刺活检病例中,取材合格可获得明确病理诊断的病例规定为合格病例。
超声引导穿刺活检取材合格率= 病理诊断明确的超声引导穿刺活检病例数 *100%
超声引导穿刺活检病例数
9.超声引导置管引流成功率
对所抽查的超声引导置管引流病例中,用置管引流成功病例数占总置管引流病例数的比例,判断超声引导置管引流的成功率。
超声引导置管引流成功率=超声引导置管引流成功病例数 x100%
总超声引导置管引流病例数

 0512-62362333
0512-62362333

